Нормальная скорость распространения пламени. Особенности процесса горения в двс с искровым зажиганием. Скорость распространения пламени Влияние различных факторов на процесс горения в двс с искровым зажиганием
1) Влажность материала.
2) Влияние ориентации образца в пространстве.
При отрицательных углах наклона (направление движение пламени сверху вниз) скорость распространения пламени или не изменяется или же слабо уменьшается. При увеличении положительного угла наклона (направление движения пламени снизу вверх) свыше 10-15 0 скорость распространения пламени резко возрастает.
3) Влияние скорости и направления воздушных потоков.
С увеличением скорости попутного ветра улучшается газообмен, уменьшается угол наклона пламени к образцу. Скорость распространения возрастает.
Поток воздуха, направленный против направления движения пламени, оказывает двоякое влияние на скорость распространения пламени.
В результате аэродинамического торможения и охлаждения прогретых участков поверхности перед фронтом пламени скорость распространения пламени снижается. С другой стороны, поток воздуха интенсифицирует смешение продуктов пиролиза с окислителем, быстрее происходит образование гомогенной горючей смеси, носик пламени приближается к поверхности твердого материала, что, в свою очередь, приводит к дальнейшему увеличению интенсивности, и это ускоряет распространение пламени.
4) Влияние геометрических размеров образца.
Различают термически толстые и термически тонкие образцы.
Термическая толщина - это толщина слоя твердого материала, прогретого перед фронтом пламени выше начальной температуры к моменту распространения пламени на данный участок поверхности.
5) Влияние материала подложки.
Если горючий материал соприкасается с материалом (подложкой), теплофизические свойства которого отличаются от воздуха, то это также будет влиять на скорость распространения пламени (наклеенная бумага, изоляция проводов и т.п.). Если l подл > l гор. мат. , то тепло будет интенсивно отводиться от образца, и скорость распространения будет меньше, чем в случае отсутствия подложки.
6) Влияние содержания кислорода в окружающей среде.
С увеличением содержания кислорода в окружающей среде скорость распространения пламени увеличивается.
7. Влияние начальной температуры образца.
Для древесины увеличение начальной температуры до 230–250 о С (температурная область пиролиза) приводит к резкому увеличению u л.
Выгорание твердых материалов
Одновременно с распространением пламени по поверхности материала начинается процесс его выгорания. Закономерности выгорания твердых материалов существенно зависят от характера превращения твердой фазы в газообразные продукты.
Если разложение твердой фазы протекает в узком приповерхностном слое без образования углистого слоя, то в этом случае горение протекает с постоянной скоростью. На поверхности твердой фазы после воспламенения устанавливается постоянная температура, равная температуре кипения или возгонки вещества.
Механизм горения твердых веществ, протекающий с образованием углистого остатка на поверхности горения, более сложен. Так горят практически все вещества растительного происхождения, некоторые пластмассы, содержащие в своем составе негорючие или трудногорючие наполнители (тальк, сажу и т.п.). К наиболее распространенным горючим веществам растительного происхождения такого типа относится древесина. В момент воспламенения за счет теплового потока от зоны пламени температура поверхностного слоя древесины быстро возрастает до 450-500 о С. Происходит интенсивное разложение веществ с образованием летучих продуктов и древесного угля, при этом температура на поверхности повышается до 600 о С.
По глубине горящей древесины имеют место области с различными физическими и физико-химическими характеристиками. Условно их можно разделить на 4 зоны:
I - древесный уголь, состоящий на 99% из углерода;
II - древесина с различной степенью пиролизованности;
III - непиролизованная, сухая древесина;
IV - исходная древесина.
По мере выделения летучих продуктов из твердой фазы при горении древесины протекает переугливание материала на все большую глубину. Рост толщины углистого слоя обусловливает повышение его термического сопротивления и, следовательно, снижает скорость прогрева и пиролиза еще не разложившихся слоев древесины, и скорость пламенного горения постепенно снижается. Пламенное горение древесины прекращается при снижении массовой скорости выделения летучих до 5 г/(м 2 ·с). Толщина слоя угля при этом достигает 15-20 мм.
Прекращение пламенного горения древесины открывает доступ кислорода воздуха к нагретому до температуры 650-700 о С углю. Начинается второй этап горения древесины - гетерогенное окисление углистого слоя в основном по реакции С + О 2 ® СО 2 + 33000 кДж/кг, температура углистого слоя возрастает до 800 о С, и процесс гетерогенного горения угля еще более интенсифицируется.
Реальная картина перехода гомогенного горения в гетерогенное несколько отличается от приведенной.
Основным количественным параметром, характеризующим процесс выгорания твердых материалов, является массовая скорость выгорания, которая представляет собой один из параметров, обусловливающих динамику пожара.
Приведенная массовая скорость выгорания представляет собой количество вещества, выгорающего в единицу времени с единицы площади пожара.
Горение металлов
По характеру горения металлы делятся на две группы: летучие и нелетучие.
Летучие металлы имеют Т пл < 1000 К, Т кип < 1500 К. К ним относятся щелочные металлы (литий, натрий, калий и др.) и щелочноземельные (магний, кальций).
Нелетучие металлы имеют Т пл >1000 К, Т кип >2500 К. Механизм горения во многом определяется свойствами оксида металла. Т пл летучих металлов ниже Т пл их оксидов. При этом последние представляют собой достаточно пористые образования.
При поднесении ИЗ к поверхности металла происходит его испарение и окисление. При достижении концентрации паров, равной нижнему концентрационному пределу воспламенения, происходит их воспламенение. Зона диффузионного горения устанавливается у поверхности, большая доля тепла передается металлу и он нагревается до Т кип. Образующиеся пары, свободно диффундируя через пористую оксидную пленку, поступают в зону горения. Кипение металла вызывает периодическое разрушение оксидной пленки, что интенсифицирует горение. Продукты горения (оксиды металлов) диффундируют не только к поверхности металла, способствуя образованию корки оксида, но и в окружающее пространство, где, конденсируясь, образуют твердые частички в виде белого дыма. Образование белого плотного дыма является визуальным признаком горения летучих металлов.
У нелетучих металлов, обладающих высокими температурами фазового перехода, при горении на поверхности образуется весьма плотная оксидная пленка, которая хорошо сцепляется с поверхностью металла. В результате этого скорость диффузии паров металла через пленку резко снижается и крупные частицы, например, алюминия и бериллия, гореть не способны. Как правило, пожары таких металлов имеют место в том случае, когда они находятся в виде стружки, порошков и аэрозолей. Их горение происходит без образования плотного дыма. Образование плотной оксидсидной пленки на поверхности металла приводит к взрыву частицы. Это явление, особенно часто наблюдающееся при движении частицы в высокотемпературной окислительной среде, связывают с накоплением паров металлов под оксидной пленкой с последующим внезапным ее разрывом. Это, естественно, приводит к резкой интенсификации горения.
Горение пылей
Пыль - это дисперсная система, состоящая из газообразной дисперсионной среды (воздух и т.д.) и твердой дисперсной фазы (мука, сахар, древесина, уголь и т.д.).
Факторы, влияющие на скорость распространения пламени по пылевоздушным смесям:
1) Концентрация пыли.
Как и в случае горения гомогенной газовоздушной смеси, максимальная скорость распространения пламени имеет место для смесей несколько выше стехиометрического состава. Для торфяной пыли это 1,0-1,5 кг/м 3 .
2) Зольность.
При увеличении зольности уменьшается концентрация горючего компонента и, соответственно, уменьшается скорость распространения пламени.
С уменьшением содержания кислорода скорость распространения пламени снижается.
Классификация пылей по взрывопожарной опасности.
По взрывопожарной опасности пыли делятся на классы:
I класс - наиболее взрывоопасная - j н до 15 г/м 3 ;
II класс - взрывоопасная - 15 г/м 3 < j н < 65 г/м 3 ;
III класс - наиболее пожароопасная - j н > 65 г/м 3 ; Т св до 250 о С;
IV класс - пожароопасная - j н > 65 г/м 3 ; Т св > 250 о С.
ДИНАМИКА РАЗВИТИЯ ПОЖАРА
Под динамикой пожара понимают совокупность законов и закономерностей, описывающих изменение основных параметров пожара во времени и пространстве. О характере пожара можно судить по совокупности большого количества его параметров: по площади пожара, по температуре пожара, скорости его распространения, интенсивности тепловыделения, интенсивности газообмена, интенсивности задымления и т. д.
Параметров пожара так много, что на одних видах пожаров одни из них являются основными, а на других - вторичными. Все зависит от того, какие цели поставлены в исследование того или иного вида пожара.
В качестве основных параметров, изменяющихся во времени, для изучения динамики пожара принимаем площадь пожара, температуру пожара, интенсивность газообмена и задымления, скорость распространения пожара. Эти параметры пожара наиболее доступны измерению, анализу, расчетам. Они служат исходными данными для определения вида необходимой техники и расчета сил и средств при тушении пожаров, проектировании автоматических систем пожаротушения и т. п.
С момента возникновения пожара, при свободном его развитии, до полного его прекращения пожар в помещении можно разделить на фазы.
Фазы пожара
I. Фаза загорания.
Пламя возникает от постороннего источника зажигания на небольшом участке и медленно распространяется. Вокруг зоны горения образуется конвективный газовый поток, который обеспечивает необходимый газообмен. Поверхность горючего материала прогревается, размер факела увеличивается, увеличивается газообмен, растет лучистый тепловой поток, который поступает в окружающее пространство и на поверхность горючего материала. Продолжительность фазы загорания колеблется от 1 до 3 мин.
II. Фаза начала пожара.
Температура среды в помещении медленно растет. Весь предыдущий процесс повторяется, но уже с большей интенсивностью. Продолжительность второго этапа примерно 5-10 мин.
III. Фаза объемного развития пожара - бурный процесс нарастания всех перечисленных параметров. Температура в помещении достигает 250 -300°С. Начинается «объемная» фаза развития пожара и фаза объемного распространения пожара. При температуре газовой среды в помещении 300°С происходит разрушение остекления. Догорание при этом может происходить и за пределами помещения (огонь вырывается из проемов наружу). Скачком изменяется интенсивность газообмена: она резко возрастает, интенсифицируется процесс оттока горячих продуктов горения и приток свежего воздуха в зону горения.
IV.Фаза пожара .
На данной фазе температура в помещении может кратковременно снизиться. Но в соответствии с изменением условий газообмена резко возрастают такие параметры пожара, как полнота сгорания, скорость выгорания и распространения процесса горения. Соответственно резко возрастает и общее тепловыделение на пожаре. Температура, несколько снизившаяся в момент разрушения остекления из-за притока холодного воздуха, резко возрастает, достигая 500 - 600 °С. Процесс развития пожара бурно интенсифицируется. Увеличивается численное значение всех ранее упомянутых параметров пожара. Площадь пожара, среднеобъемная температура в помещении (800-900 °С), интенсивность выгорания пожарной нагрузки и степень задымления достигают максимума.
V. Фаза стационарного горения.
Параметры пожара стабилизируются. Это обычно наступает на 20-25 мин пожара и, в зависимости от величины пожарной нагрузки, может длиться 20-30 мин.
VI. Фаза затухания.
Интенсивность горения постепенно снижается, т.к. основная часть пожарной нагрузки уже выгорела. В помещении накопилось большое количество продуктов горения. Среднеобъемная концентрация кислорода в помещении снизилась до 16-17 %, а концентрация продуктов горения, препятствующих интенсивному горению, возросла до предельного значения. Интенсивность лучистого переноса тепла к горючему материалу уменьшилась из-за снижения температуры в зоне горения. Из-за повышения оптической плотности среды интенсивность горения медленно снижается, что ведет к снижению всех остальных параметров пожара. Площадь пожара не сокращается: она может расти или стабилизироваться.
VII. Фаза догорания.
Для этой заключительной фазы пожара характерно медленное тление, после чего через некоторое, иногда достаточно продолжительное, время горение прекращается.
Основные параметры пожара
Рассмотрим количественно некоторые основные параметры пожара, определяющие динамику его развития. Определим интенсивность тепловыделения на пожаре, так как это один из основных параметров процесса горения:
Q=βQ р н V м ’Sп, (кДж/с)
где β и Q р н - постоянные (коэффициент недожога и низшая теплота сгорания пожарной нагрузки);
V м ¢ - приведенная массовая скорость выгорания;
S п – площадь пожара;
V м ¢ и S п зависят от времени развития пожара, темпераыура пожара, интенсивности газообмена и др.
Приведенную массовую скорость выгорания V м ¢ определяем по формуле:
v м ¢ = (а×Т п +b×I г) v м o ¢
где а, b - эмпирические коэффициенты;
v м o ¢ - приведенная массовая скорость выгорания пожарной нагрузки для данного вида горючего материала;
Т п - среднее значение температуры пожара;
I г - интенсивность газообмена.
Зависимость площади пожара от основных параметров его развития имеет вид:
S п = k (v р ∙ τ) n
где к и n – коэффициенты, зависящие от геометрической формы площади пожара;
v р – линейная скорость распространения пожара;
τ – время его свободного развития.
k = π; n = 2 k = ; n = 2 k = 2а; n = 1
k = ; n = 2 k = 2а; n = 1
Линейная скорость распространения пожара зависит от вида горючей нагрузки, средней температуры пожара и интенсивности газообмена:
v p = (а 1 T п + b 1 I г)v po
где а 1 и b 1 - эмпирические коэффициенты, устанавливающие зависимость линейной скорости распространения пожара от средней температуры и интенсивности газообмена, численное значение которых определяется опытным путем для каждого конкретного вида горючего;
v р o - линейная скорость распространения горения для данного вида горючего.
По мере развития пожара температура пожара и интенсивность газообмена будут расти, увеличивая линейную скорость распространения горения и приведенную массовую скорость выгорания.
Тепловой режим на пожаре
Возникновение и скорость протекания тепловых процессов зависят от интенсивности тепловыделения в зоне горения, т.е. от теплоты пожара. Количественной характеристикой изменения тепловыделения на пожаре в зависимости от различных условий горения служит температурный режим. Под температурным режимом пожара понимают изменение температуры во времени. Определение температуры пожара как экспериментальным, так и расчетным методами чрезвычайно сложно. Для инженерных расчетов при решении ряда практических задач температуру пожара определяют из уравнения теплового баланса. Баланс тепла на пожаре составляется не только для определения температуры пожара, но и для выявления количественного распределения тепловой энергии. В общем случае тепловой баланс пожара для данного момента времени может быть представлен следующим образом:
Q п = Q пг +Q к +Q л
где Q п - тепло, выделяющееся на пожаре, кДж;
Q пг - тепло, содержащееся в продуктах горения, кДж;
Q к - тепло, передаваемое из зоны горения конвекцией воздуху, омывающему зону, но не участвующему в горении, кДж;
Q л – тепло, передаваемое из зоны горения излучением.
Для открытых пожаров установлено, что доля тепла, передаваемого из зоны горения излучением и конвекцией, составляет 40-50% от Q п. Оставшаяся доля тепла (60-70% от Q п) идет на нагрев продуктов горения. Таким образом, 60-70% от теоретической температуры горения данного горючего материала дадут приближенное значение температуры пламени. Температура открытых пожаров зависит от теплотворной способности горючих материалов, скорости их выгорания и метеорологических условий. В среднем максимальная температура открытого пожара для горючих газов составляет 1200 - 1350°С, для жидкостей – 1100 - 1300°С и для твердых горючих материалов органического происхождения – 1100 - 1250°С.
При внутреннем пожаре на температуру влияет больше факторов: природа горючего материала, величина пожарной нагрузки и ее расположение, площадь горения, размеры здания (площадь пола, высота помещения и т.д.) и интенсивность газообмена (размеры и расположение проемов). Рассмотрим подробнее влияние перечисленных факторов.
Пожар можно разделить на три характерных периода по изменению температуры: начальный, основной и заключительный.
Начальный период - характеризуется сравнительно невысокой среднеобъемной температурой.
Основной период - в течение его сгорает 70-80 % общей нагрузки горючих материалов. Окончание этого периода происходит, когда среднеобъемная температура достигает наибольшего значения или уменьшается не более чем до 80% от максимального значения.
Заключительный период - характеризуется убыванием температуры вследствие выгорания пожарной нагрузки.

Рис 9.1. Изменение температуры внутреннего пожара во времени: 1 - кривая конкретного пожара; 2 - стандартная кривая
Поскольку скорость роста и абсолютное значение температуры пожара в каждом конкретном случае имеют свои характерные значения и особенности, введено понятие стандартной температурной кривой (рис. 21.2), обобщающей наиболее характерные особенности изменения температуры внутренних пожаров. Стандартная температура описывается уравнением.
Нормальная скорость распространения пламени - скорость перемещения фронта пламени относительно несгоревшего газа в направлении, перпендикулярном к его поверхности.
Значение нормальной скорости распространения пламени следует применять в расчетах скорости нарастания давления взрыва газо- и паровоздушных смесей в закрытом, негерметичном оборудовании и помещениях, критического (гасящего) диаметра при разработке и создании огнепреградителей, площади легко сбрасываемых конструкций, предохранительных мембран и других разгерметизирующих устройств; при разработке мероприятий по обеспечению пожаровзрывобезопасности технологических процессов в соответствии с требованиями ГОСТ 12.1.004 и ГОСТ 12.1.010.
Сущность метода определения нормальной скорости.распространения пламени заключается в приготовлении горючей смеси известного состава внутри реакционного сосуда, зажигании смеси в центре точечным источником, регистрации изменения во времени давления в сосуде и обработке экспериментальной зависимости “давление-время” с использованием математической модели процесса горения газа в замкнутом сосуде и процедуры оптимизации. Математическая модель позволяет получить расчетную зависимость “давление-время”, оптимизация которой по аналогичной экспериментальной зависимости дает в результате изменение нормальной скорости в процессе развития взрыва для конкретного испытания.
Нормальной скоростью горения называют скорость распространения фронта пламени по отношению к несгоревшим реагентам. Скорость горения зависит от ряда физико-химических свойств реагентов, в частности теплопроводности и скорости химической реакции, и имеет вполне определенное значение для каждого горючего (при постоянных условиях горения). В табл. 1 приведены скорости горения (и пределы воспламенения) некоторых газообразных смесей. Концентрации горючего в смесях определены при 25°С и нормальном атмосферном давлении. Пределы воспламенения за отмеченными исключениями получены при распространении пламени в трубе диаметром 0,05 м, закрытой с обеих сторон. Коэффициенты избытка горючего определены как отношение объемных содержаний горючего в реальной смеси к стехиометрической смеси (j1) и к смеси при максимальной скорости горения (j2).
Таблица 1
Скорости горения конденсированных смесей (неорганический окислитель + магний)
| Лист |
| № докум. |
| Подпись |
| Дата |
| Лист |
| ТГиВ 20.05.01.070000.000 ПЗ |
Как видно, при горении воздушных газовых смесей при атмоферном давлении u mах лежит в пределах 0,40-0,55 м/с, а – в пределах 0,3-0,6 кг/(м2-с). Лишь для некоторых низкомолкулярных непредельных соединений и водорода u mах лежит в пределах 0,8-3,0 м/с, а достигает 1–2 кг/ (м2с). По увеличению и mах исследованные горючие в смесях с воздухом можно
расположить в следующий ряд: бензин и жидкие ракетные топлива – парафины и ароматические соединения – оксид углерода – циклогексан и циклопропан – этилен – оксид пропилена – оксид этилена – ацетилен – водород.
| Изм. |
| Лист |
| № докум. |
| Подпись |
| Дата |
| Лист |
| ТГиВ 20.05.01.070000.000 ПЗ |
Линейная скорость горения кислородных смесей значительно выше, чем воздушных (для водорода и оксида углерода – в 2-3 раза, а для метана – больше чем на порядок). Массовая скорость горения изученных кислородных смесей (кроме смеси СО + O2) лежит в пределах 3,7-11,6 кг/(м2 с).
В табл. 1 приведены (по данным Η. А. Силина и Д. И. Постовского) скорости горения уплотненных смесей нитратов и перхлоратов с магнием. Для приготовления смесей использовали порошкообразные компоненты с размерами частиц нитратов 150-250 мкм, перхлоратов 200-250 мкм и магния 75-105 мкм. Смесью заполняли картонные оболочки диаметром 24-46 мм до коэффициента уплотнения 0,86. Образцы сгорали на воздухе при нормальных давлении и начальной температуре.
Из сопоставления данных табл. 1 и 1.25 следует, что конденсированные смеси превосходят газовые смеси по массовой и уступают им по линейной скорости горения . Скорость горения смесей с перхлоратами меньше скорости горения смесей с нитратами, а смеси с нитратами щелочных металлов горят с более высокой скоростью, чем смеси с нитратами щелочноземельных металлов.
Таблица 2
Пределы воспламенения и скорости горения смесей с воздухом (I ) и кислородом (II) при нормальном давлении и комнатной температуре
| Лист |
| № докум. |
| Подпись |
| Дата |
| Лист |
| ТГиВ 20.05.01.070000.000 ПЗ |
| Изм. |
Методы расчета скорости выгорания жидкостей
| Изм. |
| Лист |
| № докум. |
| Подпись |
| Дата |
| Лист |
| ТГиВ 20.05.01.070000.000 ПЗ |
![]() ; (16)
; (16)
где M - безразмерная скорость выгорания;
 ; (17)
; (17)
M F - молекулярная масса жидкости, кг·моль -1 ;
d - характерный размер зеркала горящей жидкости, м. Определяется как корень квадратный из площади поверхности горения; если площадь горения имеет форму окружности, то характерный размер равен ее диаметру. При расчете скорости турбулентного горения можно принять d = 10 м;
Т к - температура кипения жидкости, К.
Порядок расчета следующий.
Определяют режим горения по величине критерия Галилея Ga , вычисляемого по формуле
где g - ускорение свободного падения, м·с -2 .
В зависимости от режима горения вычисляют безразмерную скорость выгорания М . Для ламинарного режима горения:
Для переходного режима горения:
е сли , то ![]() , (20)
, (20)
если , то , (21)
Для турбулентного режима горения:
; ![]() , (22)
, (22)
M 0 - молекулярная масса кислорода, кг·моль -1 ;
n 0 - стехиометрический коэффициент кислорода в реакции горения;
n F - стехиометрический коэффициент жидкости в реакции горения.
B - безразмерный параметр, характеризующий интенсивность массопереноса, вычисляемый по формуле
![]() , (23)
, (23)
где Q - низшая теплота сгорания жидкости, кДж·кг -1 ;
| Изм. |
| Лист |
| № докум. |
| Подпись |
| Дата |
| Лист |
| ТГиВ 20.05.01.070000.000 ПЗ |
c - изобарная теплоемкость продуктов горения (принимается равной теплоемкости воздуха c = 1), кДж·кг -1 ·К -1 ;
T 0 - температура окружающей среды, принимаемая равной 293 К;
H - теплота парообразования жидкости при температуре кипения, кДж·кг -1 ;
c e - средняя изобарная теплоемкость жидкости в интервале от T 0 до T к.
Если известны кинематическая вязкость пара или молекулярная масса и температура кипения исследуемой жидкости, то скорость турбулентного горения вычисляют с использованием экспериментальных данных по формуле
где m i - экспериментальное значение скорости выгорания в переходном режиме горения, кг·м --2 ·с -1 ;
d i - диаметр горелки, в которой получено значение m i , м. Рекомендуется использовать горелку диаметром 30 мм. Если в горелке диаметром 30 мм наблюдается ламинарный режим горения, следует применять горелку большего диаметра.
Над поверхностью жидкого или твердого вещества при любой температуре существует паровоздушная смесь, давление которой в состоянии равновесия определяется давлением насыщенных паров или их концентрацией. С увеличением температуры давление насыщенных паров возрастет но экспоненциальной зависимости (уравнение Клапейрона - Клаузиса):
где Р н „ - давление насыщенного пара, Па; Q„ C11 - теплота испарения, кДж/моль; Т - температура жидкости, К.
Для любой жидкости существует интервал температур, в котором концентрация насыщенных паров над зеркалом (поверхность жидкости) будет находится в области воспламенения, т.е. НКПВ
Для создания НКПВ паров достаточно нагреть до температуры, равной НТПВ, не всю жидкость, а лишь только ее поверхностный слой.
При наличии источника зажигания такая смесь будет способна к воспламенению. Па практике чаще используют понятия «температура вспышки» и «температура воспламенения».
Температура вспышки - минимальная температура жидкости, при которой над ее поверхностью образуется концентрация паров, способная к воспламенению от источника зажигания, однако скорость образования паров недостаточна для поддержания горения.
Таким образом, как при температуре вспышки, так и при нижнем температурном пределе воспламенения над поверхностью жидкости образуется нижний концентрационный предел воспламенения, однако в последнем случае НКПВ создается насыщенными парами. Поэтому температура вспышки всегда несколько выше, чем НТПВ. Хотя при температуре вспышки наблюдается кратковременное воспламенение паров, не способное перейти в устойчивое горение жидкости, тем не менее, при определенных условиях вспышка может стать причиной возникновения пожара.
Температура вспышки принята за основу классификации жидкостей на легковоспламеняющиеся (ЛВЖ) и горючие жидкости (ГЖ). К ЛВЖ относятся жидкости, имеющие температуру вспышки в закрытом сосуде 61 °С и ниже, к горючим - с температурой вспышки более 61°С.
Экспериментально температуру вспышки определяют в приборах открытого и закрытого типа. В сосудах закрытого типа значения температуры вспышки всегда ниже, чем в открытом, поскольку в этом случае пары жидкости имеют возможность диффундировать в атмосферу и для создания горючей концентрации над поверхностью требуется более высокая температура.
В табл. 2.4 приведена температура вспышки некоторых жидкостей, определенных приборами открытого и закрытого типа.
Таблица 2.4
Температура вспышки разных видов жидкости при разных методах определения
Температура воспламенения - минимальная температура жидкости, при которой после воспламенения паров от источника зажигания устанавливается стационарное горение.
У легковоспламеняющихся жидкостей температура воспламенения выше, чем температура вспышки, на 1-5°, при этом, чем ниже температура вспышки, тем меньше разность между температурами воспламенения и вспышки.
У горючих жидкостей, имеющих высокую температуру вспышки, разница между этими температурами доходит до 25-35°. Между температурой вспышки в закрытом тигле и нижним температурным пределом воспламенения имеется корреляционная связь, описываемая формулой
Это соотношение справедливо при Г В(.
Существенная зависимость температур вспышки и воспламенения от условий эксперимента вызывает определенные трудности при создании расчетного метода оценки их величины. Одним из наиболее распространенных из них является полуэмпирический метод, предложенный В. И. Блиновым:
где Г вс - температура вспышки (воспламенения), К; Р нп - парциальное давление насыщенного пара жидкости при температуре вспышки (воспламенения), Па; D () - коэффициент диффузии паров жидкости, с/м 2 ; b - количество молекул кислорода, необходимое для полного окисления одной молекулы горючего; В - константа метода определения.
При расчете температуры вспышки в замкнутом сосуде рекомендуется принимать В = 28, в открытом сосуде В = 45; для расчета температуры воспламенения принимают В = 53.
Температурные пределы воспламенения могут быть рассчитаны:
По известным значениям температуры кипения
где ^н(в)’ 7/ип - соответственно нижний (верхний) температурный предел воспламенения и температура кипения, °С; k, I - параметры, значения которых зависят от вида горючей жидкости;
По известным значениям концентрационных пределов. Для этого сначала определяется концентрация насыщенных паров над поверхностью жидкости
где (р„ п - концентрация насыщенных паров, %; Р н п - давление насыщенных паров, Па; Р 0 - внешнее (атмосферное) давление, Па.
Из формулы (2.41) следует
Опеределив по значению нижнего (верхнего) предела воспламенения давление насыщенного пара, находим температуру, при которой это давление достигается. Она и является нижним (верхним) температурным пределом воспламенения.
По формуле (2.41) можно решать и обратную задачу: рассчитывать концентрационные пределы воспламенения по известным значениям температурных пределов.
Свойство пламени к самопроизвольному распространению наблюдается не только при горении смесей горючих газов с окислителем, но и при горении жидкостей и твердых веществ. При локальном воздействии тепловым источником, например открытым пламенем, жидкость будет прогреваться, возрастет скорость испарения и при достижении поверхностью жидкости температуры воспламенения в месте воздействия теплового источника произойдет зажигание паровоздушной смеси, установится устойчивое пламя, которое затем с определенной скоростью будет распространяться по поверхности и холодной части жидкости.
Что же является движущей силой распространения процесса горения, каков его механизм?
Распространение пламени по поверхности жидкости протекает в результате теплопередачи за счет излучения, конвекции и молекулярной теплопроводности от зоны пламени к поверхности зеркала жидкости.
По современным представлениям основной движущей силой распространения процесса горения является теплоизлучение от пламени. Пламя, обладая высокой температурой (более 1000°С), способно, как известно, излучать тепловую энергию. Согласно закону Стефана - Больцмана интенсивность лучистого теплового потока, отдаваемого нагретым телом, определяется соотношением
где ц я - интенсивность лучистого теплового потока, кВт/м 2 ; 8 0 - степень черноты тела (пламени) (е 0 = 0,75-Н,0); а = = 5,7 10 11 кДж/(м 2 с К 4) - постоянная Стефана - Больцмана; Г г - температура тела (пламени), К; Г 0 - температура среды, К.
Тепло, излучаясь во все стороны, частично поступает и на еще не загоревшиеся участки поверхности жидкости, прогревая их. При повышении температуры поверхностного слоя над прогретым участком процесс испарения жидкости интенсифицируется и образуется паровоздушная смесь. Как только концентрация паров жидкости превысит НКВП, произойдет ее зажигание от пламени. Затем уже этот участок поверхности жидкости начинает интенсивно прогревать соседний участок поверхности жидкости и т.д. Скорость распространения пламени по жидкости зависит от скорости прогрева поверхности жидкости лучистым тепловым потоком от пламени, т.е. от скорости образования горючей паровоздушной смеси над поверхностью жидкости, которая, в свою очередь, зависит от природы жидкости и начальной температуры.
Каждый вид жидкости имееют свою теплоту испарения и температуру вспышки. Чем выше их значения, тем более длительное время необходимо для ее прогрева до образования горючей паровоздушной смеси, тем, следовательно, ниже скорость распространения пламени. С увеличением молекулярной массы вещества в пределах одного гомологического ряда снижается давление паров упругости, возрастают теплота испарения и температура вспышки, соответственно снижается скорость распространения пламени.
Увеличение температуры жидкости повышает скорость распространения пламени, так как время, необходимое для прогрева жидкости до температуры вспышки перед зоной горения, уменьшается.
При вспышке скорость распространения пламени по зеркалу жидкости будет (по физическому смыслу) равна скорости распространения пламени по паровоздушной смеси состава, близкого к НКПВ, т.е. 4-5 см/с. При увеличении начальной температуры жидкости выше температуры вспышки скорость распространения пламени будет зависеть (аналогично скорости распространения пламени) от состава горючей смеси. Действительно, при увеличении температуры жидкости выше температуры ее вспышки концентрация паровоздушной смеси над поверхностью зеркала будет расти от НКВП до 100% (температура кипения).
Следовательно, вначале при повышении температуры жидкости от температуры вспышки до температуры, при которой над поверхностью образуются насыщенные пары, с концентрацией, равной стехиометрической (точнее, несколько выше, чем стехиометрическая), скорость распространения пламени будет нарастать. В закрытых сосудах по мере дальнейшего повышения температуры жидкости скорость распространения пламени начинает снижаться, вплоть до скорости, соответствующей верхнему температурному пределу воспламенения, при котором распространение пламени но паровоздушной смеси станет уже невозможным из-за недостатка кислорода в паровоздушной смеси над поверхностью жидкости. Над поверхностью же открытого резервуара концентрация паров на разных уровнях будет различной: у поверхности она будет максимальной и соответствовать концентрации насыщенного пара при данной температуре, по мере увеличения расстояния от поверхности концентрация постепенно будет снижаться из-за конвективной и молекулярной диффузии.
При температуре жидкости, близкой к температуре вспышки, скорость распространения пламени по поверхности жидкости будет равна скорости его распространения по смеси паров в воздухе на НКПВ, т.е. 3-4 см/с. При этом фронт пламени будет расположен у поверхности жидкости. При дальнейшем увеличении начальной температуры жидкости скорость распространения пламени будет расти аналогично росту нормальной скорости распространения пламени по паровоздушной смеси с увеличением ее концентрации. С максимальной скоростью пламя будет распространяться по смеси с концентрацией, близкой к стехиометрической. Следовательно, с увеличением начальной температуры жидкости выше Г стх скорость распространения пламени будет оставаться постоянной, равной максимальному значению скорости распространения горения по стехиометрической смеси или несколько больше ее (рис. 2.5). Таким образом,

Рис. 25.
1 - горение жидкости в закрытой емкости; 2 - горение жидкости в открытой емкости при изменении начальной температуры жидкости в открытой емкости в широком диапазоне температур (вплоть до температуры кипения) скорость распространения пламени будет изменяться от нескольких миллиметров до 3-4 м/с.
С максимальной скоростью пламя будет распространяться по смеси с концентрацией, близкой к стехиометрической. С увеличением температуры жидкости выше Г стх увеличится расстояние над жидкостью, на котором сформируется стехиометрическая концентрация, а скорость распространения пламени останется прежней (см. рис. 2.5). Это обстоятельство всегда надо помнить, как при организации профилактической работы, так и при тушении пожаров, когда, например, может возникнуть опасность подсоса воздуха в закрытую емкость - ее разгерметизация.
После возгорания жидкости и распространения пламени но ее поверхности устанавливается диффузионный режим ее выгорания , который характеризуется удельной массовой W rM и линейной W V Jl скоростями.
Удельная массовая скорость - масса вещества, выгорающего с единицы площади зеркала жидкости в единицу времени (кг/(м 2 *с)).
Линейная скорость - расстояние, на которое перемещается уровень зеркала жидкости в единицу времени за счет ее выгорания (м/с).
Массовая и линейная скорости выгорания взаимосвязаны через плотность жидкости р:
После воспламенения жидкости температура ее поверхности повышается от температуры воспламенения до кипения, происходит формирование прогретого слоя. В этот период скорость выгорания жидкости постепенно повышается, растет высота факела пламени в зависимости от диаметра резервуара и вида горючей жидкости. После 1-10 мин горения наступает стабилизация процесса: скорость выгорания и размеры пламени остаются в дальнейшем неизменными.
Высота и форма пламени при диффузионном горении жидкости и газа подчиняются одним и тем же закономерностям, поскольку в обоих случаях процесс горения определяется взаимной диффузией горючего и окислителя. Однако если при диффузионном горении газов скорость струи газа не зависит от процессов, протекающих в пламени, то при горении жидкости устанавливается определенная скорость выгорания, которая зависит как от термодинамических параметров жидкости, так и от условий диффузии кислорода воздуха и паров жидкости.
Между зоной горения и поверхностью жидкости устанавливается определенный тепло- и массообмен (рис. 2.6). Часть теплового потока, поступающего к поверхности жидкости q 0y затрачивается на ее нагрев до температуры кипения q ucn . Кроме того, тепло q CT на нагрев жидкости поступает от факела пламени через стенки резервуара за счет теплопроводности. При достаточно большом его диаметре величиной q CT можно прене- бречь, тогда q {) = K „ n +
Очевидно, что
где с - теплоемкость жидкости, кДжДкг-К); р - плотность жидкости, кг/м 3 ; W nc - скорость роста прогретого слоя, м/с; W Jl - линейная скорость выгорания, м/с; 0и СП - теплота парообразования, кДж/кг; Г кип - температура кипения жидкости, К.

Рис. 2.6.
Г () - начальная температура; Г кип - температура кипения;
Т г - температура горения; q KUW q Jl - соответственно конвективный и лучистый тепловые потоки; q 0 - тепловой поток, поступающий на поверхность жидкости
Из формулы (2.45) следует, что интенсивность теплового потока из зоны пламени обусловливает определенную скорость поставки горючего в эту зону, химическое взаимодействие которого с окислителем, в свою очередь, влияет на величину # 0 . В этом и состоит взаимосвязь массо- и теплообмена зоны пламени и конденсированной фазы при горении жидкостей и твердых веществ.
Оценку доли тепла от общего тепловыделения при горении жидкости, которая затрачивается на ее подготовку к горению q 0 , можно провести в следующей последовательности.
Принимая для простоты W rjl = W nx , получим
Скорость тепловыделения с единицы поверхности зеркала жидкости (удельную теплоту пожара q ll7K) можно определить по формуле
где Q H - низшая теплота сгорания вещества, кДж/кг; Р п - коэффициент полноты сгорания.
Тогда, учитывая состояние (2.44) и разделив выражение (2.45) на формулу (2.46), получим
Расчеты показывают, что около 2% от общего тепловыделения при горении жидкости затрачивается на образование и доставку паров жидкости в зону горения. При установлении процесса выгорания температура поверхности жидкости увеличивается до температуры кипения, которая в дальнейшем остается неизменной. Данное утверждение относится к индивидуальной жидкости. Если же рассматривать смеси жидкостей, имеющих разную температуру кипения, то сначала происходит выход легкокипящих фракций, затем - все более высококипящих.
На скорость выгорания значительное влияние оказывает прогрев жидкости по глубине в результате передачи тепла от нагретой лучистым потоком q 0 поверхности жидкости в ее глубь. Этот теплоперенос осуществляется за счет теплопроводности и конвенции.
Прогрев жидкости за счет теплопроводности может быть представлен экспоненциальной зависимостью вида
где Т х - температура слоя жидкости на глубине х, К; Г кип - температура поверхности (температура кипения), К; k - коэффициент пропорциональности, м -1 .
Такой тип температурного поля называется распределением температуры первого рода (рис. 2.7).
Ламинарная конвенция возникает в результате различной температуры жидкости у стенок резервуара и в его центре, а также вследствие фракционной разгонки в верхнем слое при горении смеси.
Дополнительная передача тепла от нагретых стенок резервуара к жидкости приводит к прогреву ее слоев у стенок до более высокой температуры, чем в центре. Более нагретая у стенок жидкость (или даже пузырьки пара в случае ее прогрева у стенок выше температуры кипения) поднимается вверх, что способствует интенсивному промешиванию и быстрому прогреву жидкости на большой глубине. Образуется так называемый гомотермический слой, т.е. слой с практически постоянной температурой, толщина которого увеличивается во время горения. Такое температурное поле называют распределением температуры второго рода.

Рис. 2.7.
1 - распределение температуры первого рода; 2 - распределение температуры второго рода
Образование гомотермического слоя возможно также и в результате фракционной перегонки приповерхностных слоев смеси жидкостей, имеющих различную температуру кипения. По мере выгорания таких жидкостей приповерхностный слой обогащается более плотными высококипя- щими фракциями, которые опускаются вниз, способствуя гем самым конвективному прогреву жидкости.
Установлено, что чем ниже температура кипения жидкости (дизельное топливо, трансформаторное масло), гем труднее образуется гомотермический слой. При их горении температура стенок резервуара редко превышает температуру кипения. Однако при горении влажных высококипя- щих нефтепродуктов вероятность образования гомотермического слоя достаточна высокая. При прогреве стенок резервуара до 100°С и выше образуются пузырьки водяного пара, которые, устремляясь вверх, вызывают интенсивное перемещение всей жидкости и быстрый прогрев в глубине. Зависимость толщины гомотермического слоя от времени горения описывается соотношением
где х - толщина гомотермического слоя на некоторый момент времени горения, м; х пр - предельная толщина гомотермического слоя, м; т - время, отсчитываемое от момента начала формирования слоя, с; р - коэффициент, с -1 .
Возможность образования достаточно толстого гомотермического слоя при горении влажных нефтепродуктов чревата возникновением вскипания и выброса жидкости.
Скорость выгорания существенно зависит от вида жидкости, начальной температуры, влажности и концентрации кислорода в атмосфере.
Из уравнения (2.45) с учетом выражения (2.44) можно определить массовую скорость выгорания:

Из формулы (2.50) очевидно, что на скорость выгорания оказывают влияние интенсивность теплового потока, поступающего от пламени к зеркалу жидкости, и теплофизические параметры горючего: температура кипения, теплоемкость и теплота испарения.
Из табл. 2.5 очевидно, что существует определенное соответствие между скоростью выгорания и затратами тепла на прогрев и испарения жидкости. Так, в ряду бен- золксилолглицеринов с увеличением затрат тепла на прогрев и испарение скорость выгорания снижается. Однако при переходе от бензола к диэтиловому эфиру затраты тепла уменьшаются. Это кажущееся несоответствие обусловлено различием в интенсивности тепловых потоков, поступающих от факела к поверхности жидкости. Лучистый поток достаточно велик для коптящего пламени бензола и мал для относительно прозрачного пламени диэтилового эфира. Как правило, соотношение скоростей выгорания наиболее быстро горящих жидкостей и наиболее медленно горящих достаточно невелико и составляет 3,0-4,5.
Таблица 25
Зависимость скорости выгорания от затрат тепла на прогрев и испарение
Из выражения (2.50) следует, что с увеличением Г 0 скорость выгорания возрастает, поскольку снижаются затраты тепла на прогрев жидкости до температуры кипения.
Содержание влаги в смеси понижает скорость выгорания жидкости, во-первых, вследствие дополнительных затрат тепла на ее испарение, а во-вторых, в результате флегмати- зирующего влияния паров воды в газовой зоне. Последнее приводит к снижению температуры пламени, а следовательно, согласно формуле (2.43), уменьшается и его излучающая способность. Строго говоря, скорость выгорания влажной жидкости (жидкости, содержащей воду) не постоянна, она увеличивается или уменьшается в процессе горения в зависимости от температуры кипения жидкости.
Влажное горючее может быть представлено как смесь двух жидкостей: горючее + вода, в процессе горения которых происходит их фракционная разгонка. Если температура кипения горючей жидкости меньше температуры кипения воды (100°С), то происходит преимущественное выгорание горючего, смесь обогащается водой, скорость выгорания снижается и, наконец, горение прекращается. Если температура кипения жидкости больше 100°С, то, наоборот, сначала преимущественно испаряется влага и концентрация ее снижается. В результате скорость выгорания жидкости возрастает, вплоть до скорости горения чистого продукта.
Как правило, с повышением скорости ветра скорость выгорания жидкости увеличивается. Ветер интенсифицирует процесс смешивания горючего с окислителем, тем самым повышая температуру пламени (табл. 2.6) и приближая пламя к поверхности горения.
Таблица 2.6
Влияние скорости ветра на температуру пламени
Все это повышает интенсивность теплового потока, поступающего на нагрев и испарение жидкости, следовательно, приводит к увеличению скорости выгорания. При большей скорости ветра пламя может сорваться, что приведет к прекращению горения. Так, например, при горении тракторного керосина в резервуаре диаметром 3 м наступал срыв пламени при скорости ветра 22 м/с.
Большинство жидкостей не могут гореть в атмосфере с содержанием кислорода менее 15%. С увеличением концентрации кислорода выше этого предела скорость выгорания растет. В атмосфере, значительно обогащенной кислородом, горение жидкости протекает с выделением большого количества сажи в пламени и наблюдается интенсивное кипение жидкой фазы. Для многокомпонентных жидкостей (бензин, керосин и т.н.) температура поверхности с увеличением содержания кислорода в окружающей среде растет.
Повышение скорости выгорания и температуры поверхности жидкости с ростом концентрации кислорода в атмосфере обусловлено увеличением излучающей способности пламени в результате роста температуры горения и высокого содержания сажи в нем.
Скорость выгорания также значительно меняется с понижением уровня горючей жидкости в резервуаре: происходит снижение скорости выгорания, вплоть до прекращения горения. Поскольку подвод кислорода воздуха из окружающей среды внутрь резервуара затруднен, то при понижении уровня жидкости увеличивается расстояние h np между зоной пламени и поверхностью горения (рис. 2.8). Лучистый поток к зеркалу жидкости уменьшается, а следовательно, уменьшается и скорость выгорания, вплоть до затухания. При горении жидкостей в резервуарах большого диаметра предельная глубина /г пр, при которой происходит затухание горения, очень большая. Так, для резервуара с диаметром 5 м она составляет 11 м, а с диметром Им - около 35 м.

Горение -это интенсивные химические окислительные реакции, которые сопровождаются выделением тепла и свечением. Горение возникает при наличии горючего вещества, окислителя и источника воспламенения. В качестве окислителей в процессе горения могут выступать кислород, азотная кислота. В качестве горючего - многие органические соединения, сера, сероводород, колчедан, большинство металлов в свободном виде, оксид углерода, водород и т.д.
В условиях реального пожара окислителем в процессе горения обычно является кислород воздуха. Внешнее проявление горения-пламя, которое характеризуется свечением и выделением тепла. При горении систем, состоящих только из твердых или жидких фаз или их смесей, пламя может и не возникать, т. е. происходит беспламенное горение или тление.
В зависимости от агрегатного состояния исходного вещества и продуктов горения различают гомогенное горение, горение взрывчатых веществ, гетерогенное горение.
Гомогенное горение. При гомогенном горении исходные вещества и продукты горения находятся в одинаковом агрегатном состоянии. К этому типу относится горение газовых смесей (природного газа, водорода и т. п. с окислителем-обычно, кислородом воздуха)/
Горение взрывчатых веществ связано с переходом вещества из конденсированного состояния в газ.
Гетерогенное горение. При гетерогенном горении исходные вещества (например твердое или жидкое горючее и газообразный окислитель) находятся в разных агрегатных состояниях. Важнейшие технологические процессы гетерогенного горения-горение угля, металлов, сжигание жидких топлив в нефтяных топках, двигателях внутреннего сгорания, камерах сгорания ракетных двигателей.
Движение пламени по газовой смеси называется распространением пламени. В зависимости от скорости распространения пламени горения может быть дефлаграционным со скоростью несколько м/с, взрывным-скорость порядка десятков и сотен м/с и детонационным-тысячи м/с.
Дефлаграционное горение подразделяется на ламинарное и турбулентное.
Ламинарному горению присуща нормальная скорость распространения пламени.
Нормальной скоростью распространения пламени, называется скорость перемещения фронта пламени относительно несгоревшего газа, в направлении, перпендикулярном к его поверхности.
Температура относительно слабо увеличивает нормальную скорость распространения пламени, инертные примеси уменьшают ее, а повышение давления ведет либо к повышению, либо к снижению скорости.
В ламинарном газовом потоке скорости газов малы. Скорость горения в этом случае зависит от скорости образования горючей смеси. В турбулентном пламени завихрение газовых струй улучшает перемешивание реагирующих газов, так как увеличивается поверхность, через которую происходит молекулярная диффузия.
Показатели пожаро-взрывоопасности газов. Их характеристика и область применения
Пожароопасность технологических процессов в значительной степени определяется физико-химическими свойствами обращающихся в производстве сырья, промежуточных и конечных продуктов.
Показатели пожаро- и взрывоопасности используются при категорировании помещений и зданий, при разработке систем для обеспечения пожарной безопасности и взрывобезопасности.
Газы-вещества, абсолютное давление паров которых при температуре 50 °С равно или более 300 кПа или критическая температура которых менее 50 °С.
Для газов применимы след.показатели:
Группа горючести -показатель, который применим для всех агрегатных состояний.
Горючесть-способность вещества или материала к горению. По горючести вещества и материалы подразделяются на три группы.
Негорючие (несгораемые)-вещества и материалы, неспособные к горению на воздухе. Негорючие вещества могут быть пожароопасными (например, окислители, а также вещества, выделяющие горючие продукты при взаимодействии с водой, кислородом воздуха или друг с другом).
Трудногорючие (трудносгораемые) -вещества и материалы, способные возгораться в воздухе от источника зажигания, но не способные самостоятельно гореть после его удаления.
Горючие (сгораемые) -вещества и материалы, способные самовозгораться, а также возгораться от источника зажигания и самостоятельно гореть после его удаления. Из группы горючих веществ и материалов выделяют легковоспламеняющиеся вещества и материалы.
Легковоспламеняющимися называют горючие вещества и материалы, способные воспламеняться от кратковременного (до 30 с) воздействия источника зажигания с низкой энергией (пламя спички, искра, тлеющая сигарета и т. п.).
Горючесть газов определяют косвенно: газ, имеющий концентрационные пределы воспламенения в воздухе, относят к горючим; если газ не имеет концентрационных пределов вопламенения, но самовоспламеняется при определенной темпе ратуре, его относят к трудногорючим; при отсутствии концентрационных пределов воспламенения и температуры самовоспламенения газ относят к негорючим.
На практике группу горючести используют для подразделения материалов по горючести, при установлении классов взрывоопасных и пожароопасных зон по ПУЭ, при определении категории помещений и зданий по взрывопожарной и пожарной опасности, при разработке мероприятий для обеспечения пожаро- и взрывобезопасности оборудования и помещений.
Температура самовоспламенения - самая низкая температура вещества, при которой в условиях специальных испытаний происходит резкое увеличение скорости экзотермических реакций, заканчивающихся пламенным горением.
Концентрационные пределы распространения пламени (воспламенения) - тот интервал концентраций, в котором возможно горение смесей горючих паров и газов с воздухом или кислородом.
Нижний (верхний) концентрационный предел распространения пламени - минимальное (максимальное) содержание горючего в смеси горючее вещество-окислительная среда» при котором возможно распространение пламени по смеси на любое расстояние от источника зажигания. Внутри этих пределов смесь горюча, а вне их-смесь гореть неспособна.
Температурные пределы распространения пламени (воспламенения)-такие температуры вещества, при которых его насыщенные пары образуют в конкретной окислительной среде концентрации, равные соответственно нижнему (нижний температурный предел) и верхнему (верхний температурный предел) концентрационным пределам распространения пламени.
Способность взрываться и гореть при взаимодействии с водой, кислородом воздуха и другими веществами - качественный показатель,который характеризует особую пожарную опасность некоторых веществ. Это свойство веществ применяют при определении категории производств, а также при выборе безопасных условий проведения технологических процессов и условий совместного хранения и транспортирования веществ и материалов.
Скорость ламинарного горения – скорость с которой фронт пламени перемещается в направлении перпендикулярном к поверхности свежей ТВС.
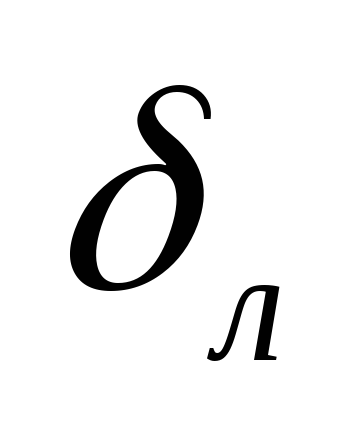 –зона ламинарного
горения;
–зона ламинарного
горения;
 –скорость
ламинарного горения.
–скорость
ламинарного горения.
Турбулентное горение.

Турбулентная скорость пламени – скорость, с которой фронт пламени перемещается в турбулезированном потоке.
 –зона турбулентного
горения;
–зона турбулентного
горения;

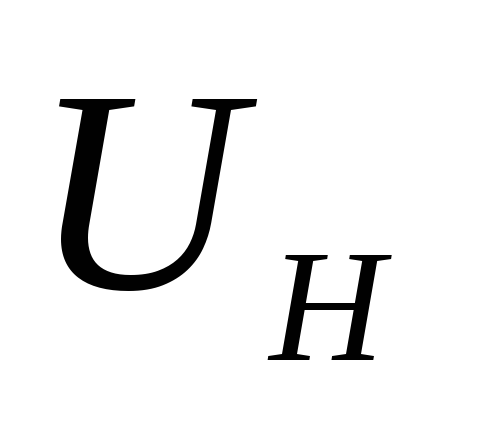 –нормальные
скорости маленьких частиц.
–нормальные
скорости маленьких частиц.
Ламинарное горение не обеспечивает необходимую скорость выделения тепла в двигателе, поэтому требуется турбулезация газового потока.
Уравнение
Аррениуса:
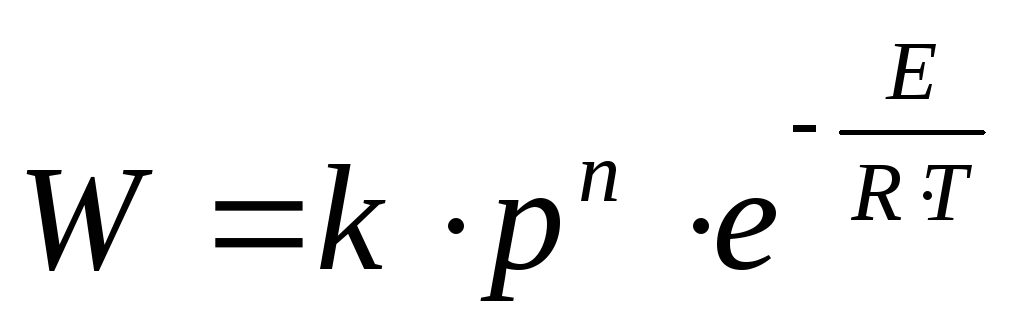 – скорость химической реакции.
– скорость химической реакции.
 –константа
химической реакции, зависящая от состава
смеси и рода топлива;
–константа
химической реакции, зависящая от состава
смеси и рода топлива;
 –давление химической
реакции;
–давление химической
реакции;
 –порядок химической
реакции;
–порядок химической
реакции;

 –универсальная
газовая постоянная;
–универсальная
газовая постоянная;
 –температура
химической реакции;
–температура
химической реакции;
 –энергия активации
– энергия, необходимая для разрыва
внутримолекулярных связей.
–энергия активации
– энергия, необходимая для разрыва
внутримолекулярных связей.
Влияние различных факторов на процесс горения в двс с искровым зажиганием.
Состав смеси.

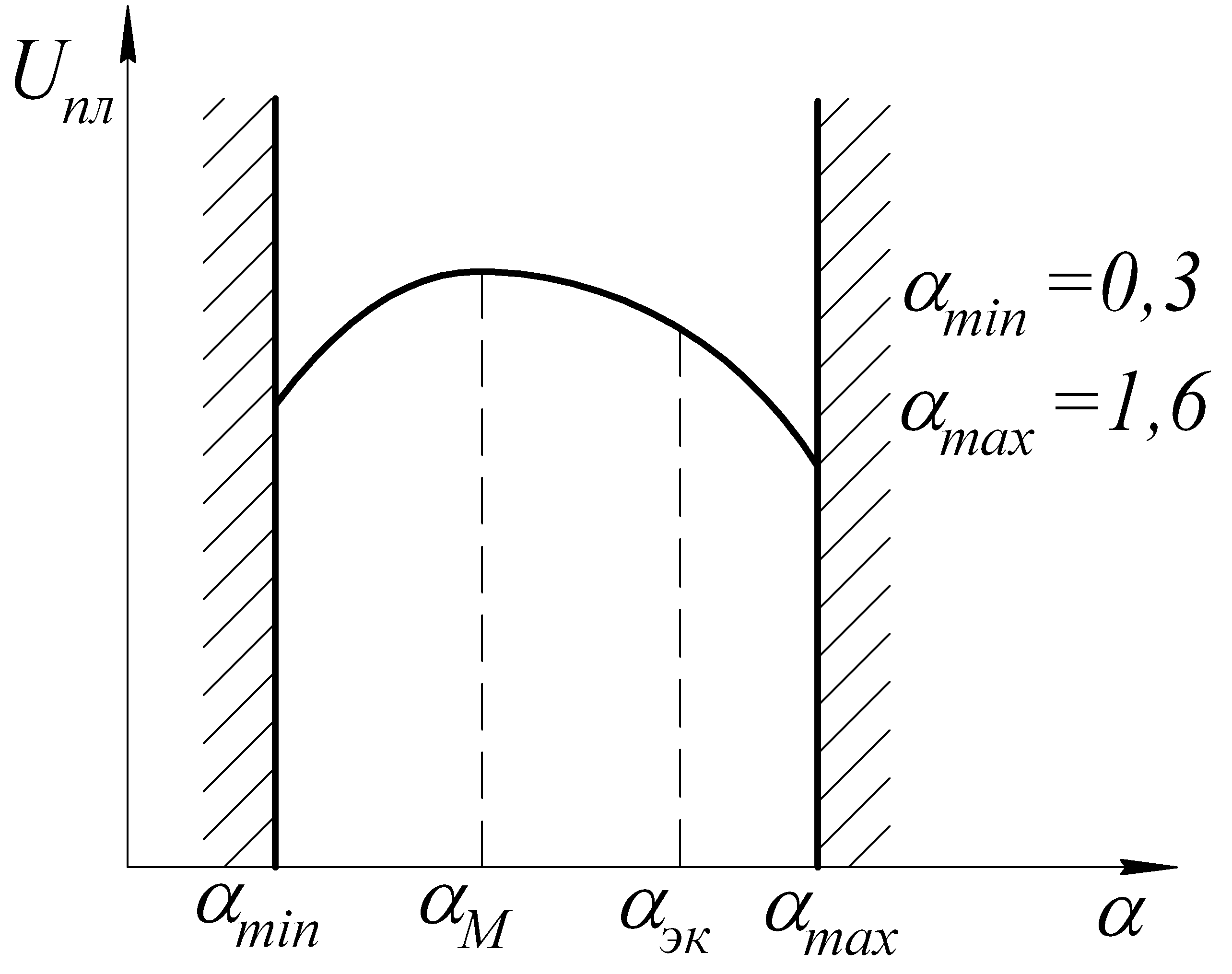 –верхний
концентрационный предел;
–верхний
концентрационный предел;
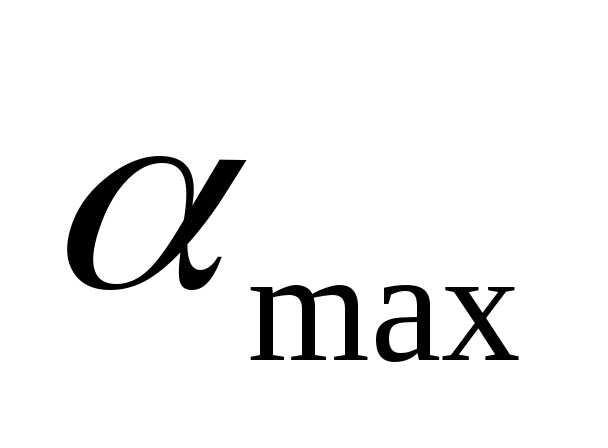 –нижний
концентрационный предел;
–нижний
концентрационный предел;
 –нормальное
горение;
–нормальное
горение;

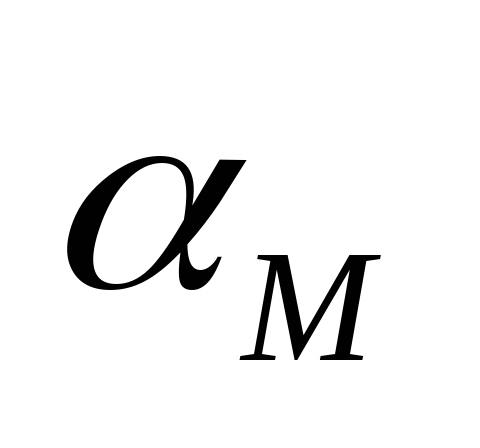 –мощностной
состав смеси
– максимальная мощность, развиваемая
двигателем.
–мощностной
состав смеси
– максимальная мощность, развиваемая
двигателем.

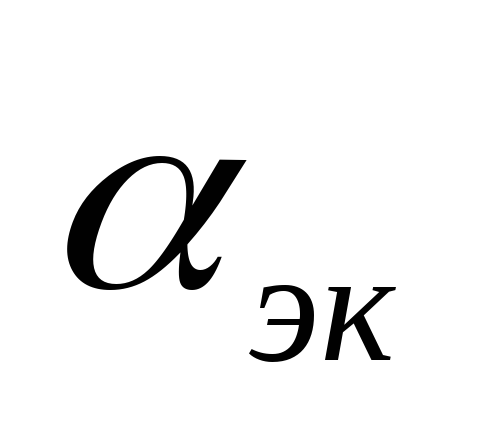 –экономический
состав смеси
– максимальная экономичность.
–экономический
состав смеси
– максимальная экономичность.
Степень сжатия.



С увеличение частоты
оборотов, увеличивается фаза воспламенения,
что приводит к позднему развитию процесса
сгорания и уменьшению количества тепла
выделившегося за цикл. Поэтому при
изменении
 требуется регулирование угла опережения
зажигания (УОЗ).
требуется регулирование угла опережения
зажигания (УОЗ).
Угол опережения зажигания.
Угол опережения зажигания – угол поворота коленвала от момента подачи искры до ВМТ.
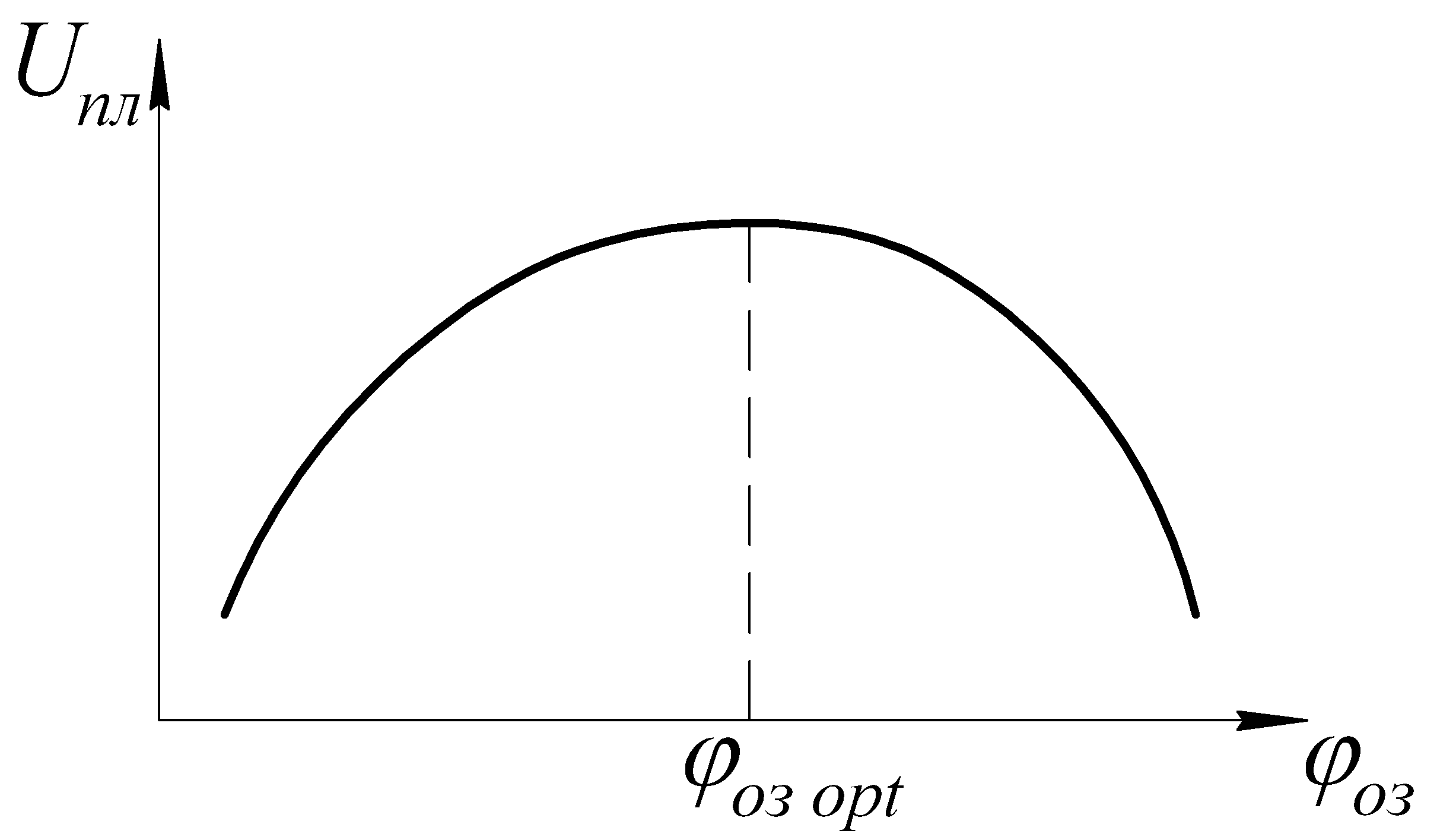
П од
нагрузкой
понимают угол поворота дроссельной
заслонки – именно ей регулируют нагрузку
на двигатель.
од
нагрузкой
понимают угол поворота дроссельной
заслонки – именно ей регулируют нагрузку
на двигатель.
 –угол поворота
дроссельной заслонки.
–угол поворота
дроссельной заслонки.
Основные нарушения процесса горения в двс с искровым зажиганием. Детонация.
Д етонация
– взрывообразное горение смеси,
сопровождающееся ударными волнами
давления, распространяющимися по объему
камеры сгорания. Детонация возникает
в результате самовоспламенения удаленных
от свечи участков смеси, вследствие
интенсивного нагрева и сжатия при
распространении фронта пламени.
етонация
– взрывообразное горение смеси,
сопровождающееся ударными волнами
давления, распространяющимися по объему
камеры сгорания. Детонация возникает
в результате самовоспламенения удаленных
от свечи участков смеси, вследствие
интенсивного нагрева и сжатия при
распространении фронта пламени.

При детонации:

Отражаясь от стенок камеры сгорания, ударная волна образует вторичные фронты пламени и очаги самовоспламенения. Внешне детонация проявляется в виде глухих стуков при работе двигателя на больших нагрузках.
Последствия работы двигателя с детонацией:
Перегрев и прогорание отдельных узлов двигателя (клапаны, поршни, прокладки головки, электроды свечей);
Механические разрушения деталей двигателя вследствие ударных нагрузок;
Снижение мощности и экономичности работы.
Т.о. длительная работа с детонацией недопустима.
П еречислим
факторы, вызывающие детонацию:
еречислим
факторы, вызывающие детонацию:

Способность топлива к самовоспламенению характеризует детонационная стойкость , а детонационная стойкость оценивается октановым числом (ОЧ) .
ОЧ – численно равно объемной доли плохо дитонирующего изооктана смеси с легко дитонирующим нормальным гептаном, эквивалентным по детонационным свойствам данному бензину.
Изооктан – 100 ед., нормальный гептан – 0 ед.
Например: октановое число 92 означает, что данный бензин обладает такой же детонационной стойкостью как эталонная смесь из 92% изооктана и 8% нормального гептана.
А – автомобильный бензин;
– автомобильный бензин;
и – исследовательский метод получения бензина;
м – моторный метод (буква обычно не пишется).
В моторном методе исследования регулируют степень сжатия, пока не начнется детонация, и определяют по таблицам октановое число.
Моторные методы имитируют движение на полной нагрузке (грузовик за городом).
Исследовательский метод имитирует движение при частичной нагрузке (в городе).


Если октановое число избыточно велико, то снижается скорость распространения пламени. Процесс сгорания затягивается, что приводит к снижению КПД и повышению температуры отработавших газов. Следствием этого является падение мощности, повышение расхода топлива, перегрев двигателя и прогорание отдельных элементов. Максимальные показатели двигателя достигаются при октановом числе топлива близком к порогу детонации.
Способы борьбы с детонацией: